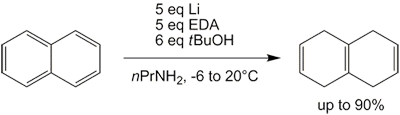Birchni kamaytirish - Birch reduction
| Birchni kamaytirish | |
|---|---|
| Nomlangan | Artur Birch |
| Reaksiya turi | Organik oksidlanish-qaytarilish reaktsiyasi |
| Identifikatorlar | |
| Organik kimyo portali | qayinni kamaytirish |
| RSC ontologiya identifikatori | RXNO: 0000042 |
The Birchni kamaytirish konvertatsiya qilish uchun ishlatiladigan organik reaktsiya arenalar ga sikloheksadienlar. Reaksiya avstraliyalik kimyogar nomi bilan atalgan Artur Birch. Bunda organik reduksiya ning aromatik halqalar suyuqlikda ammiak bilan natriy, lityum, yoki kaliy va an spirtli ichimliklar, kabi etanol va tert-butanol. Bu reaktsiya mumkin emas katalitik gidrogenlash odatda aromatik halqani a ga qadar kamaytiradi sikloheksan.[1][2]
Masalan, ning kamayishi naftalin:[3]
Asosiy reaktsiya mexanizmi
Natriyning suyuq ammiakdagi eritmasi quyidagilardan iborat elektrid tuz [Na (NH3)x]+ e−, juda zich ko'k rangga ega. The solvatlangan elektronlar a berish uchun aromatik halqaga qo'shing radikal anion. Kiritilgan alkogol protonni radikal anionga va shuningdek oldingi karbanionga etkazib beradi; ko'pgina substratlar uchun ammiak etarli darajada kislotali emas.[4]

Regioelektivlik
Anizolning kamayishi eng oddiy misollardan biridir va 1-tenglamada ko'rsatilgan. Benzo kislotasining kamayishi 2-tenglamada ko'rsatilgan.
Ringda joylashgan joy radikal anion dastlab protonlangan bo'lib, mahsulot tuzilishini aniqlaydi. Metoksi (MeO) kabi elektron donor bilan alkil protonatsiyasi ba'zi tekshiruvchilar tomonidan orto (ya'ni qo'shni yoki 1,2) o'rnini bosuvchi. Boshqa tergovchilar protonatsiya deb o'ylashgan meta (1,3) o'rnini bosuvchi. Artur Birch buni ma'qulladi meta protonatsiya. Elektronni olib qo'yadigan substituentlar bilan protonatsiya o'rnini bosuvchi joyda (ipso) yoki paragraf (1,4), lekin bu ham noaniq. A. J. Birchning empirik qoidalarida donor o'rnini bosuvchi moddalar uchun yakuniy mahsulotda so'nggi qo'shaloq bog'lanishlar bo'yicha maksimal miqdordagi o'rinbosarlar bo'lishi aytilgan. Elektronni tortib oluvchi guruhlar uchun mahsulotning er-xotin bog'lanishlari o'rnini bosuvchilardan qochadi. Reaksiya paytida va yakuniy mahsulotda guruhlarni joylashtirish afzalligi regioselektivlik deb nomlanadi.


Reaksiya mexanizmining umumiy tafsilotlari
Metallni ammiakdagi eritmasi ta'minlaydi elektronlar ular aromatik halqa tomonidan qabul qilinib, reaktsiyaning birinchi bosqichida mos keladigan B radikal anionini hosil qiladi. Buning ortidan sikloheksadienil radikalini hosil qilish uchun alkogolning protonatsiyasi bilan sikloheksadienil radikalini hosil qiladi.Shundan keyin ikkinchi elektron radikalga ko'chib sikloheksadienil karbanion D hosil qiladi. Oxirgi bosqichda ikkinchi proton sikloheksadienil karbanionni birlashtirilmagan sikloheksadienil mahsuloti. Ushbu qadamlar anizol uchun quyida keltirilgan.

Reaksiya ma'lum uchinchi tartib - birinchi tartib aromatik, birinchi tartib ishqoriy metallda, birinchi tartib spirtli ichimliklarda.[5] Buning uchun stavkani cheklovchi qadam B radikal anionining sikloheksadienil radikaliga S ga aylanishi.
Reaktsiyaning regioselektivligi
Birch qisqarishi bir nechta murakkab mexanik xususiyatlarga ega. Ushbu xususiyatlar reaktsiyani boshqaradi regioelektivlik va quyida ko'rib chiqiladi. Metoksil yoki alkil kabi elektron donorlarga ega bo'lgan aromatik moddalar uchun Birchning qoidasi shundan iboratki, mahsulot maksimal miqdordagi substitentlarga ega bo'lgan qoldiq er-xotin bog'lanishlarga ega bo'ladi. Karboksil kabi elektronni tortib oluvchi guruhlarga ega bo'lgan aromatik moddalar uchun o'rnini bosuvchi guruhlar er-xotin bog'lanishdan qochishadi. Ikkala holatda ham, elektron xayr-ehson qilish va qaytarib olish guruhlari bilan, qoldiq er-xotin bog'lanishlar birlashtirilmaydi (pastga qarang). Ushbu regioselektivlikni hisobga oladigan reaksiya mexanizmlari katta ilmiy qiziqish mavzusi. Asosiy xususiyatlar:
- Suyuq ammiakdagi gidroksidi metallar eriydi va "oddiy" deb o'ylangan ko'k eritmani beradi.erkin elektronlar ". Elektronlar aromatik halqa tomonidan birma-bir qabul qilinadi. Birinchi elektron so'rilib bo'lgach, radikal anion hosil bo'ladi. Keyin spirtli molekula yangi gidroksil vodorodini beradi C-H aloqasi; bu vaqtda a radikal shakllangan. Buning ortidan a berish uchun ikkinchi elektron olinadi karbanion sikloheksadienil tipidagi (ya'ni salbiy zaryadli olti a'zoli halqada C = C – C – C = C bilan). Unda bu sikloheksadienil anion bo'ladi protonli mavjud spirtli ichimliklar tomonidan. Protonatsiya sikloheksadienil tizimining markazida sodir bo'ladi. Bu (regio-) selektivlik xarakterlidir.
- Dastlab radikal anion protonlangan joyda mahsulotning tuzilishini aniqlaydi. Metoksi (MeO) kabi elektron donor yoki alkil guruhi bilan protonatsiya ba'zi tadqiqotchilar tomonidan o'ylangan orto (ya'ni qo'shni yoki 1,2) o'rnini bosuvchi. Boshqa tergovchilar protonatsiya deb o'ylashgan meta (1,3) o'rnini bosuvchi. Artur Birch buni ma'qulladi meta protonatsiya. Elektronni olib qo'yadigan substituentlar bilan protonatsiya o'rnini bosuvchi joyda (ipso) sodir bo'ladi yoki paragraf (1,4). Shunga qaramay, turli xil fikrlar mavjud. A. J. Birchning empirik qoidalarida donor o'rnini bosuvchi moddalar uchun yakuniy mahsulotda so'nggi qo'shaloq bog'lanishlar bo'yicha eng ko'p miqdordagi o'rinbosarlar bo'lishi aytilgan. Elektronni tortib oluvchi guruhlar uchun mahsulotning er-xotin bog'lanishlari o'rnini bosuvchilardan qochadi. Mexanizmda va yakuniy mahsulotda guruhlarni joylashtirish afzalligi regioselektivlik deb nomlanadi.
- Reaksiya mexanizmi reaktsiya o'tishi bilan molekulyar o'zgarishlarning tafsilotlarini beradi. Xayriya guruhlari holatida, A. J. Birchning afzalligi meta radikal anionning protonatsiyasi sifatli mulohazalarga asoslangan edi, ammo bu tajribada isbotlanmagan.
- 1961 yilda radikal anionning elektron zichligini oddiy hisoblash natijasida uning ekanligini aniqladi orto eng salbiy bo'lgan va shuning uchun protonatsiya qilish ehtimoli yuqori bo'lgan sayt. Bundan tashqari, ikkinchi protonatsiya hisoblanmasdan sikloheksadienil anion markazida paydo bo'lib, konjuge bo'lmagan mahsulot hosil qiladi.
- Kimyoviy adabiyotdagi noaniqlik endi faqat tarixiy ahamiyatga ega. Darhaqiqat, ba'zi bir keyingi hisoblash natijalari haqida xabar berilgan bo'lib, ular afzallik berishdan farq qiladi meta aralashmasini taklif qiladigan radikal-anion protonatsiyasi orto va meta protonatsiya.[iqtibos kerak ]
- 1990 va 1993 yillarda buni ko'rsatadigan ezoterik test ishlab chiqildi orto radikal anionning protonatsiyasi afzalroq edi meta (ettidan bittagacha).[iqtibos kerak ] Bunga zamonaviyroq hisob-kitoblar ham qo'shildi. Ham tajriba, ham hisob-kitoblar 1961 yil boshidagi hisob-kitoblarga mos edi.
- Elektronlarni tortib oluvchi guruhlar bilan adabiyotda so'nggi protonlashdan oldin karbanionning xususiyatini ko'rsatadigan misollar mavjud,[iqtibos kerak ] boshlang'ich radikal-anion protonatsiyasi sodir bo'lishini ochib beradi paragraf olib qo'yiladigan substituentga.
- Muhokama uchun qolgan narsa sikloheksadienil anionning oxirgi protonatsiyasidir. 1961 yilda oddiy Gyckel hisoblashlari turli protonatsiya joylarini ajrata olmaganligi aniqlandi.[iqtibos kerak ] Biroq, hisob-kitoblar biroz aniqroq taxminlar bilan o'zgartirilganda, Gyckel hisob-kitoblari markaziy uglerodni afzal ko'rdi. 1990 va 1993 yillardagi zamonaviy hisob-kitoblar kelishilgan edi.[iqtibos kerak ]
Mexanizm
Birchni kamaytirish mexanizmi ko'p munozaralarga sabab bo'ldi. Birchni kamaytirishning asl mexanizmi radikal anionning protonatsiyasini chaqirdi meta halqa metoksi va alkil guruhlariga. Bundan tashqari, tsikloheksadienil anionning oxirgi bosqichi - protonatsiyasi sodir bo'lgan deb taxmin qilingan orto ushbu o'rinbosarlarga nisbatan. Birchning asl mexanizmi sifatli fikrlashga asoslangan edi, ya'ni radikal anion elektron zichligi, elektron qo'shilishi natijasida hosil bo'lgan, eng yuqori bo'ladi meta odatdagidan qochish sababli elektron donorga (masalan, metoksi yoki metil) orto-paragraf neytral turlarda yuqori zichlik.[6]
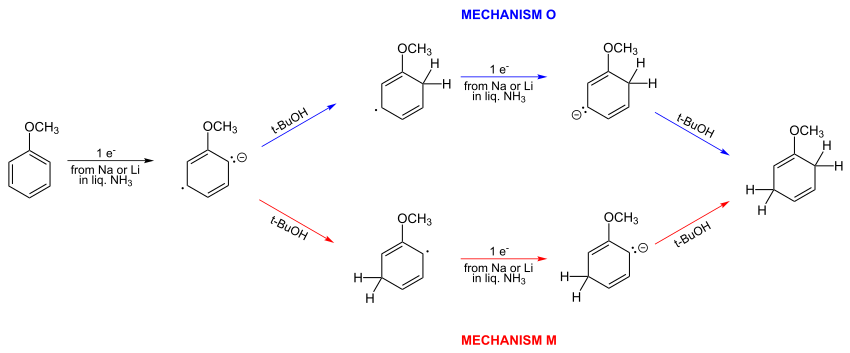
1961 yilda oddiy Gyckel hisoblashlar Birchning taklif qilgan mexanizmi noto'g'ri ekanligini ko'rsatdi. To'g'ri mexanizm O quyida tasvirlangan.[7][8]O va M ikkita a-priori alternativ mexanizmlari:
Birch bu xulosani qabul qilmadi va taklifini davom ettirdi meta radikal anionning protonatsiyasi. U taklif qildi meta hujum "qarshi chiqishidan kelib chiqadi orto va paragraf dastlabki to'lov ".[9] 1959 yilda Iknerner tomonidan sifatli dalillar keltirildi meta-xavfsizlik[5] ilgari Birch tomonidan taklif qilinganidek.
1969 yilda Burnxem protonatsiya asosan sodir bo'lishi mumkin emas degan xulosaga keldi orto holati va reaktsiyasi, ehtimol, meta holati, lekin ikkala saytda ham shunga o'xshash stavkalarda sodir bo'lishi mumkin.[10]
Keyinchalik, Birch, sharh maqolasida,[11] o'sha paytda to'g'ri mexanizmni ajratib turadigan eksperimental usul mavjud emasligini ta'kidladi. Ammo u Burnxem tomonidan nashr etilganiga e'tibor qaratdi[10] yoqimli meta hujum.
1980 nashrlarida Birch hamkorlik qildi Leo Radom da elektron zichligi degan xulosaga kelgan tadqiqotda orto va meta biroz yaqinroq bo'lgan pozitsiyalar orto afzalligi, ammo aralashmalari bilan orto va meta protonatsiya sodir bo'ladi.[12][13] Cheklangan Xartri-Fok usuli ustida slater turi orbital (3-g) va Cheklanmagan Hartree-Fock slater tipidagi orbital xuddi shu asosda o'rnatilgan hisob-kitoblardan foydalanilgan va ikkalasi ham orto va meta almashtirishlar biroz ustunlik bilan sodir bo'ladi orto.[12][13]
Eksperimental sinov va hisoblash yo'li bilan tekshirish
So'ngra 1990 va 1993 yillarda anizol va toluol radikal anionining protonlangan yoki yo'qligini eksperimental ravishda baholash usuli ishlab chiqildi. orto yoki meta.[14][15] Ezoterik usul izotoplarning selektivligi protium-deuterium muhitidagi protonatsiyada birinchi protonatsiya pog'onasining radikal anioni uchun oldingi bosqich karbanionidan kattaroq bo'lar edi. Sababi shundaki, karbanionlar mos keladigan radikal anionlarga qaraganda ancha asoslidir va shu tariqa protonatsiyada ekzotermik va kamroq tanlangan reaksiyaga kirishadi. Eksperimental ravishda kamroq deyteriy borligi aniqlandi orto saytga qaraganda meta turli xil metoksillangan aromatiklarga (1: 7) olib keldi. Bu radikal anion protonatsiyasining katta selektivligi natijasidir. Eksperimental kuzatuvlar bilan birlashtirilgan elektronlar zichligini hisoblashlari (masalan, ROHF / 6-31g). Shuningdek, chegara orbital zichligi yo'qligi aniqlandi va bundan avvalgi ba'zi hisobotlarda foydalanilgan.
Keyinchalik, 1992 va 1996 yillarda Birch ikki marta nashr etishni taklif qilmoqda meta protonatsiyaga ustunlik berildi.[16][17] Bu uning Leo Radom bilan nashr etilgan avvalgi qarashlarining teskari tomoni edi.
Biroq, Birchni kamaytirish mexanizmi bo'yicha nashr etilgan darsliklarda ta'kidlangan orto dastlabki radikal anionning protonatsiyasiga afzallik beriladi.[18]
Elektronni chiqaradigan substituentlar bilan qayinni kamaytirish
Elektron donorlik o'rnini bosuvchi moddalar misollaridan farqli o'laroq, chekinish guruhlari bilan bog'liq ish aniqroq ko'rinadi. Shunday qilib, quyida tasvirlanganidek, oldingi D dionionning tuzilishi alkilgalogenidlar tomonidan ushlanib qolishi bilan tavsiflanadi.
Benzoik kislotalarni kamaytirish mexanizmi, shu jumladan mumkin bo'lgan alkillanish

Ushbu dionion alkogolni kamaytirishda ishlatiladimi yoki yo'qligidan qat'iy nazar natijalar beradi. Shunday qilib dastlabki protonatsiya tert- butil spirt yoki ammiak paragraf B dan S gacha bo'lgan qadamda ko'rinadigan ipso emas.[19][20][21]
Qayinni regiokimyo bilan kamaytirishning ikkinchi bosqichi, konjuge bo'lmagan sikloheksadienlarni berish
Birchni kamaytirishning ikkinchi bosqichi birlashtirilmagan sikloheksadienlar ham mexanik savollar tug'diradi. Shunday qilib quyidagi rasmda ko'rsatilgandek karbanion uchun uchta rezonansli B, C va D tuzilmalar mavjud. Oddiy Hückel hisob-kitoblari, quyidagi jadvalning birinchi qismida qayd etilganidek, uchta atom 1, 3 va 5 dagi elektronlarning zichligiga teng bo'lishiga olib keladi. Ammo zichlikdan farqli o'laroq, Gyckel hisoblashi unchalik sodda emas. obligatsiyalar bo'yicha buyurtmalar,[7][22][23] va 2-3 va 5-6-bandlar jadvalning birinchi yozuvida ko'rsatilgandek qisqartiriladi. Mulliken-Uelend-Mann hisob-kitobida oddiy almashinuv integrallarini o'zgartirgan obligatsiyalar buyurtmalari bilan markaziy atom 1 da elektron zichligi eng katta bo'lishiga erishildi.[22][23] Keyinchalik zamonaviy RHF hisob-kitoblari xuddi shu natijaga olib keladi.[14][15]
Ikkinchi pog'onaning karbanioni uchun benzol va 3 ta rezonans tuzilishga elektron kirish va konjuge bo'lmagan dienni berish uchun markaziy protonatsiya:

Sikloheksadienil anionning beshta uglerodi.[22][23]
| Yaqinlashish | Zichlik Atomi 3 | Zichlik Atomi 2 | Zichlik Atomi 1 | Obligatsiya buyurtmasi 2-3 | Obligatsiya buyurtmasi 1-2 |
|---|---|---|---|---|---|
| Gyckel (taxminan 1-chi) | 0.333 | 0.00 | 0.333 | 0.788 | 0.578 |
| 2-chi | 0.317 | 0.00 | 0.365 | 0.802 | 0.564 |
| 3-chi | 0.316 | 0.00 | 0.368 | 0.802 | 0.562 |
Markaziy anion protonatsiyasi uchun ma'lum pretsedentlar mavjud.[7][24] Shunday qilib, C = CC = CO- sifatida konjuge qilingan enolatlar bir muncha vaqtdan buyon enol emas, balki anion emas, tur sharoitida ol, b-to'yinmagan karbonil birikmasini olish uchun enolat tizimining markazida kinetik ravishda protonlanadigan sifatida ma'lum bo'lgan. protonli.
Qayin alkilatsiyasi
An huzurida alkil galogenid The karbanion ham o'tishi mumkin nukleofil almashtirish bilan uglerod-uglerod aloqasi shakllanish. Almashtirilgan aromatik birikmalarda an elektronni chiqaradigan substituent, masalan karboksilik kislota,[25] barqarorlashtiradi a karbanion va eng kam almashtirilgan olefin hosil bo'ladi. Bilan elektron donorlik o'rnini bosuvchi teskari ta'sirga erishiladi.[26] Reaksiya barqarorroq bo'lganidan ko'ra kamroq termodinamik barqaror konjuge bo'lmagan 1,4 qo'shilgan mahsulotni hosil qiladi uyg'unlashgan 1,3-dien, chunki konjuge pentadienil anion oraliq mahsulotining HOMO ning eng katta orbital koeffitsienti markaziy uglerod atomida. Hosil bo'lgan 1,4-sikloheksadien hosil bo'lgandan keyin termodinamik jihatdan ancha barqaror mahsulotga muvozanat keltira olmaydi; shuning uchun kuzatilgan kinetik mahsulot ishlab chiqariladi. Kabi xavfsizroq ishqoriy metall alternativalari M-SG kamaytiruvchi vosita, shuningdek mavjud.
Yilda Qayin alkilatsiyasi The anion Qayin qisqarishida hosil bo'lgan mos keladigan tuzoqqa tushadi elektrofil kabi a haloalkane, masalan:[27]
Quyida tasvirlangan reaktsiyada 1,4-dibromobutan qo'shiladi tert-butil benzoat, alkillangan 1,4-sikloheksadien mahsulotini hosil qiladi:[28]
O'zgarishlar
Suyuq ammiak kolbada kondensatsiyalanishi va reaksiya tugagandan so'ng bir kechada bug'lanib ketishi kerakligi sababli, protsedura juda qiyin va ko'p vaqt talab qilishi mumkin. Shu bilan birga, muqobil erituvchilar ishlatilgan, masalan THF[29][30] shuningdek, aralashmasi n-propilamin va etilendiamin,[31] ham taqqoslanadigan natijalar bilan. Ikkinchisi aslida ning modifikatsiyasi Benkeser reaktsiyasi, u naftalinni oktahidro- va dekahidronaftalene qadar kamaytirishga intiladi.
Naftalanning izotetralinga (1,4,5,8-tetrahidronaftalin) kamayishi natijasida ba'zi bir moddalar hosil bo'ladi. tetralin (1,2,3,4-tetrahidronaftalen) yon mahsulot sifatida, odatdagi Birch qisqarishida bo'lgani kabi.
Kamaytirishni tashqi potentsial qurbonlik anodi (magniy yoki alyuminiy) bilan ta'minlash mumkin. Dimetilüre, proton donori, oraliqni lityum ionlari bilan (tuzlardan) barqarorlashtiradi. [32]
Tarix
Reaksiya hisobga olinadi Artur Birch Da ishlayotganda (1915-1995) Dyson Perrins laboratoriyasi da Oksford universiteti,[6][33][34][35][36][37] Voster va Godfri tomonidan 1937 yilda nashr etilgan avvalgi asarlar asosida.[38] U o'zgartiradi aromatik birikmalar ega bo'lish benzenoid uzuk mahsulotga, 1,4-sikloheksadienlar, unda ikkita vodorod atomi molekulaning qarama-qarshi uchlariga biriktirilgan.
1944 yilda Birch tomonidan bildirilgan asl reaktsiya ishlatilgan natriy va etanol.[6][33][34] Alfred L. Uaylds keyinchalik lityum yaxshi hosil berishini aniqladi.[39][40]
Qo'shimcha o'qish
- Keyn, D. (1976). "Suyuq ammiakdagi a, b-to'yinmagan karbonil birikmalarining metallarga kamayishi va u bilan bog'liq reaktsiyalar". Org. Javob bering. (ko'rib chiqish). 23: 1–258. doi:10.1002 / 0471264180.or023.01. ISBN 0471264180.
Shuningdek qarang
Adabiyotlar
- ^ Rabideau, P. V.; Martsinov, Z. (1992). "Aromatik birikmalarning qayinning kamayishi". Org. Javob bering. (ko'rib chiqish). 42: 1–334. doi:10.1002 / 0471264180.or042.01. ISBN 0471264180.
- ^ Mander, L. N. (1991). "Metall eritish va boshqa usullar bilan aromatik halqalarni qisman kamaytirish". Kompr. Org. Sintez. (ko'rib chiqish). 8: 489–521. doi:10.1016 / B978-0-08-052349-1.00237-7. ISBN 978-0-08-052349-1.
- ^ Vogel, E .; Klug, V.; Breuer, A. (1974). "1,6-Metano [10] annulen". Organik sintezlar.; Jamoa hajmi, 6
- ^ Mart, Jerri (1985), Ilg'or organik kimyo: reaktsiyalar, mexanizmlar va tuzilish (3-nashr), Nyu-York: Uili, ISBN 0-471-85472-7
- ^ a b Krapcho, A. P.; Bothner-By, A. A. (1959). "Benzol va almashtirilgan benzollarni metall-ammiak-spirtli ichimliklarni kamaytirish kinetikasi1". J. Am. Kimyoviy. Soc. 81 (14): 3658–3666. doi:10.1021 / ja01523a042.
- ^ a b v Birch, A. J. (1944). "Metalllarni eritib kamaytirish. I qism". J. Chem. Soc.: 430. doi:10.1039 / JR9440000430.
- ^ a b v Zimmerman, H. E. (1961). "Metall ammiakni kamaytirishdagi yo'nalish". Tetraedr. 16 (1–4): 169–176. doi:10.1016/0040-4020(61)80067-7.
- ^ "Asosiy katalizlangan qayta tashkil etish", "Molekulyar qayta tashkil etish" ning 6-bobi, Zimmerman, H. E., Ed. P. DeMayo, Interscience, 345-406, Nyu-York, 1963 yil.
- ^ Birch, A. J .; Nasipuri, D. (1959). "Metall-ammiak eritmalarini kamaytirishdagi reaksiya mexanizmlari". Tetraedr. 6 (2): 148–153. doi:10.1016/0040-4020(59)85008-0.
- ^ a b Burnham, D. R. (1969). "Anisolni qayinning kamayishi mexanizmidagi yo'nalish". Tetraedr. 25 (4): 897–904. doi:10.1016/0040-4020(69)85023-4.
- ^ Birch, A. J .; Subba Rao, G. (1972). Adv. Org. Kimyoviy. 8: 1–65. Yo'qolgan yoki bo'sh
sarlavha =(Yordam bering) (va u erda) - ^ a b Birch, A. J .; Xinde, A. L .; Radom, L. (1980). "Birchni kamaytirishga nazariy yondoshish. Almashtirilgan benzollarning radikal anionlarining tuzilishi va barqarorligi". J. Am. Kimyoviy. Soc. 102 (10): 3370–3376. doi:10.1021 / ja00530a012.
- ^ a b Birch, A. J .; Radom, L. (1980). "Birchni kamaytirishga nazariy yondoshish. Sikloheksadienil radikallarining tuzilishi va barqarorligi". J. Am. Kimyoviy. Soc. 102 (12): 4074–4080. doi:10.1021 / ja00532a016.
- ^ a b Zimmerman, H. E.; Vang, P. A. (1990). "Birchni kamaytirishning regioselektivligi". J. Am. Kimyoviy. Soc. 112 (3): 1280–1281. doi:10.1021 / ja00159a078.
- ^ a b Zimmerman, H. E.; Vang, P. A. (1993). "Birchni kamaytirishning regioselektivligi". J. Am. Kimyoviy. Soc. 115 (6): 2205–2216. doi:10.1021 / ja00059a015.
- ^ Birch, A. J. (1992). "Steroid gormonlar va Luftwaffe. Strategik tadqiqotlar olib boradigan korxona va uning ba'zi oqibatlari: Birchning kamayishi tug'ilishning kamayishiga aylanadi". Ukol. 57 (8): 363–377. doi:10.1016 / 0039-128X (92) 90080-S. PMID 1519267. S2CID 24827957. (bilan mexanizmni ko'rsatdi meta)
- ^ Birch, A. J. (1996). "Organik sintezdagi qayinning kamayishi". Sof Appl. Kimyoviy. 68 (3): 553–556. doi:10.1351 / pac199668030553. S2CID 41494178. (hali ham taklif qiladi meta)
- ^ "Ilg'or organik kimyo: reaktsiyalar va sintez", Frensis A. Keri, Richard J. Sundberg, p. 437
- ^ Bachi, J. V.; Epshteyn, Y .; Gertsberg-Minzli, X.; Loewnenthal, J. E. (1969). "Gibberellik kislota bilan bog'liq birikmalar sintezi. III. Gibberellinlarning halqa a analoglari". J. Org. Kimyoviy. 34: 126–135. doi:10.1021 / jo00838a030.
- ^ Taber, D. F .; Gunn, BP; Ching Chiu, I (1983). "Anionning alkillanishi o-anisid kislotasini qayinning kamayishi bilan: 2-geptil-2-sikloheksenon". Organik sintezlar. 61: 59.; Jamoa hajmi, 7, p. 249
- ^ Guo, Z .; Shultz, A. G. (2001). "Organik sintez metodikasi. 3-o'rnini bosuvchi 2-metil-2,3-dihidroizoindol-1-ni qayinning reduktsion-alkilatsiyasini tayyorlash va diastereoselektiv usulda tayyorlash". J. Org. Kimyoviy. 66 (6): 2154–2157. doi:10.1021 / jo005693g. PMID 11300915.
- ^ a b v Zimmerman, Xovard E (1975). Organik kimyogarlar uchun kvant mexanikasi. Nyu-York: Academic Press. pp.154–5. ISBN 0-12-781650-X.
- ^ a b v Zimmerman, H. E. "Molekulyar qayta tashkil etish", De Mayo, P. Ed., Interscience, Nyu-York, 1963, 350-352 betlar.
- ^ Paufler, R. M. (1960) t.f.n. Tezis, Shimoliy-G'arbiy Universitet, Evanston, IL.
- ^ Kuehne, M. E .; Lambert, B. F. (1963). "1,4-Dihidrobenzoy kislota". Organik sintezlar.; Jamoa hajmi, 5, p. 400
- ^ Paket, L. A .; Barret, J. H. (1969). "2,7-dimetiloksepin". Organik sintezlar.; Jamoa hajmi, 5, p. 467
- ^ Taber, D. F .; Gunn, B. P .; Ching Chiu, I. (1983). "O-Anisik kislota: 2-Geptil-2-sikloheksenonning qayinning qaytarilishidan anionning alkillanishi". Organik sintezlar.; Jamoa hajmi, 7, p. 249
- ^ Clive, Derrick L. J. & Sunasee, Rajesh (2007). "Benzo-birlashtirilgan karbotsikllarni aromatik halqa ustiga rasmiy radikal tsiklizatsiya bilan hosil qilish". Organik xatlar. 9 (14): 2677–2680. doi:10.1021 / ol070849l. PMID 17559217.
- ^ Ekzeri, Zoltan va Myuller, Miklos (1961). "Ishqoriy metallar bilan D2 vitaminini kamaytirish". Magyar Kémiai Folyóirat. 67: 330–332.
- ^ Donohoe, Timoti J. va Xaus, Devid (2002). Lityum di- yordamida aromatik birikmalarning ammiaksiz qisman qisqarishitert-butilbifenil (LiDBB) ". Organik kimyo jurnali. 67 (14): 5015–5018. doi:10.1021 / jo0257593. PMID 12098328.
- ^ Garst, Maykl E .; Lloyd J.; Shervin; N. Endryu; Natali S.; Alfred A .; va boshq. (2000). "Kam molekulyar og'irlikdagi aminlar va etilenediamin tarkibidagi litiy bilan kamayish". Organik kimyo jurnali. 65 (21): 7098–7104. doi:10.1021 / jo0008136. PMID 11031034.
- ^ Piters, Bayron K.; Rodriguez, Kevin X.; Reysberg, Sulaymon H.; Beil, Sebastyan B.; Xiki, Devid P.; Kavamata, Yu; Kollinz, Maykl; Starr, Jeremi; Chen, Longrui; Udyavara, Sagar; Klunder, Kevin; Gori, Timoti J.; Anderson, Skott L.; Neyrok, Metyu; Minteer, Shelli D.; Baran, Fil S. (21 fevral, 2019 yil). "Li-ionli akkumulyator kimyosidan kelib chiqqan holda kengaytiriladigan va xavfsiz sintetik organik elektroeduktsiya". Ilm-fan. 363 (6429): 838–845. doi:10.1126 / science.aav5606. PMC 7001862. PMID 30792297. Xulosa.
- ^ a b Birch, A. J. (1945). "Metalllarni eritib kamaytirish. II qism". J. Chem. Soc.: 809. doi:10.1039 / jr9450000809.
- ^ a b Birch, A. J. (1946). "Metalllarni eritib kamaytirish. III qism". J. Chem. Soc.: 593. doi:10.1039 / jr9460000593.
- ^ Birch, A. J. (1947). "Metalllarni eritib kamaytirish. IV qism". J. Chem. Soc.: 102. doi:10.1039 / jr9470000102.
- ^ Birch, Artur J. (1947). "Metalllarni eritib kamaytirish. V qism". J. Chem. Soc.: 1642. doi:10.1039 / jr9470001642.
- ^ Birch, A. J .; Mukherji, S. M. (1949). "Metalllarni eritib qaytarish. VI qism. Sintezda ba'zi qo'llanmalar". J. Chem. Soc.: 2531. doi:10.1039 / jr9490002531.
- ^ Voster, C. B.; Godfrey, K. L. (1937). "Ishqoriy metallar va suv bilan to'yinmagan aralashmalarni kamaytirish mexanizmi". Amerika Kimyo Jamiyati jurnali. 59 (3): 596. doi:10.1021 / ja01282a504.
- ^ Uaylds, A. L .; Nelson, N. A. (1953). "Fenol efirlarini dihidro hosilalari va to'yinmagan ketonlarga kamaytirishning eng yaxshi usuli". J. Am. Kimyoviy. Soc. 75 (21): 5360–5365. doi:10.1021 / ja01117a064.
- ^ Birch, A. J .; Smit, H. (1958). "Metall-amin eritmalari bilan kamaytirish: sintezdagi qo'llanmalar va tuzilishini aniqlash". Kvart. Rev. (ko'rib chiqish). 12 (1): 17. doi:10.1039 / qr9581200017.