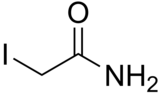
Iodatsetamid - Iodoacetamide
 | |
 | |
| Ismlar | |
|---|---|
| IUPAC nomi afzal 2-yodosetamid | |
| Identifikatorlar | |
3D model (JSmol ) | |
| ChEMBL | |
| ChemSpider | |
| ECHA ma'lumot kartasi | 100.005.119 |
| EC raqami |
|
PubChem CID | |
| RTECS raqami |
|
| UNII | |
CompTox boshqaruv paneli (EPA) | |
| |
| |
| Xususiyatlari | |
| C2H4MenNO | |
| Molyar massa | 184.964 g · mol−1 |
| Tashqi ko'rinishi | oq kristallar (sariq rang yod borligini bildiradi) |
| Erish nuqtasi | 94 ° C (201 ° F; 367 K) |
| Xavf | |
| Xavfsizlik ma'lumotlari varaqasi | MSDS 1, MSDS 2 |
| NFPA 704 (olov olmos) | |
Boshqacha ko'rsatilmagan hollar bundan mustasno, ulardagi materiallar uchun ma'lumotlar keltirilgan standart holat (25 ° C [77 ° F], 100 kPa da). | |
| Infobox ma'lumotnomalari | |
2-yodosetamid bu alkillash agenti uchun ishlatilgan peptid xaritalash maqsadlari. Uning harakatlari xuddi shunga o'xshash yodoatsetat. Odatda kovalent ravishda bog'lash uchun ishlatiladi tiol guruhi sistein shuning uchun oqsil hosil bo'lmaydi disulfid birikmalari.[1][2] Shuningdek, ishlatilgan hamma joyda ning inhibitori sifatida o'rganadi deubikuitinaza fermentlari (DUB), chunki u DUB faol uchastkasidagi sistein qoldiqlarini alkillashtiradi.
Peptidaza inhibitori
Yodoatsetamid barcha sistein peptidazalarning qaytarilmas inhibitori bo'lib, inhibisyon mexanizmi katalitik sistein qoldig'ining alkillanishidan kelib chiqadi (sxemaga qarang). Yodatsetamid kislota hosilasi bilan taqqoslaganda ancha tezroq reaksiyaga kirishadi. Ushbu kuzatuv standart kimyoviy reaktivlikka qarama-qarshi bo'lib ko'rinadi, ammo katalitik gistidinning musbat imidazolium ioni va yodoatsetatning salbiy zaryadlangan karboksil-guruhi o'rtasida o'zaro ta'sirning mavjudligi yodoatsetamidning nisbiy faolligining oshishiga sabab bo'ladi.[3]

Proteinli mass-spektrometriya
Odatda de novo (peptid) sekanslash uchun namuna tayyorlash paytida foydalaniladi oqsil massasi spektrometriyasi, ammo so'nggi tanqidchilar undan foydalanishdan qochishni taklif qilishmoqda [4]
Adabiyotlar
- ^ Smit The CV (1936). "Yodoatsetat va yodoatsetamidning turli xil sulfidril guruhlari bilan, Urease va xamirturush preparatlari bilan reaktsiyalari". J. Biol. Kimyoviy. 114 (3): 601–12.
- ^ Anson ML (1940). "Yod va yodatsetamidning mahalliy tuxum albuminlari bilan reaktsiyalari". J. Gen. Fiziol. 23 (3): 321–31. doi:10.1085 / jgp.23.3.321. PMC 2237930. PMID 19873158.
- ^ Polgar, L (1979). "Deuterium izotoplarining papain asilatsiyasiga ta'siri. Umumiy asos katalizining etishmasligi va fermentlarni qoldiruvchi guruh uchun dalillar. O'zaro ta'sir". Yevro. J. Biokimyo. 98 (2): 369–374. doi:10.1111 / j.1432-1033.1979.tb13196.x. PMID 488108.
- ^ Myuller (2017). "Proteinlarni kamaytirish va alkilatsiyani tizimli ravishda baholash yodli reaktivlar tomonidan o'ziga xos bo'lmagan nojo'ya ta'sirlarni ochib beradi". Molekulyar va uyali proteomika. 16 (7): 1173–1187. doi:10.1074 / mcp.M116.064048. PMC 5500753. PMID 28539326.

